一、团队介绍:
上海工程技术大学化学化工学院医药前沿技术研究院药理学研究团队组建于2021年。团队成员包括教授1人、讲师3人,以及在读研究生数人。通过药理学与生物信息学、病理生理学、生物化学和生物制药等多学科联合攻关,团队总体定位是围绕心血管系统疾病及恶性肿瘤发生发展中的重点、难点问题,开展疾病发病机制、药物作用新靶点及创新防治药物研发工作,以改善防治水平,促进医药领域的发展。团队研究方向包括心血管系统疾病(心肌肥厚、心肌缺血再灌注损伤、心律失常等)的发病机制研究、药物作用靶点机制研究、肿瘤药理学及非编码RNA成药性等研究。团队成员都曾主持或参加国家重点基础研究发展计划(973计划);国家自然科学基金面上项目等项目,目前承担上海市心脑血管非编码RNA成药性前沿科学研究基地(培育)建设;并在Circulation、J Clin Invest、Cardiovascular Research等国际知名杂志发表高水平科研论文。
研究方向1:心血管系统疾病的发病机制研究
将生物信息技术、人工智能大数据及生物学技术相结合,深入解析心血管系统疾病的分子网络机制,发现新型干预靶点,突破心血管疾病的药物研发瓶颈,有利于提高心脑血管系统疾病的整体防治水平。团队系列研究表明微小核苷酸(miRNA)对心脏结构重构以及电重构过程具有重要调控作用。包括miR-26a、miR-101,miR-1,miR 328,let-7d等micro RNA在小鼠房颤、传导阻滞、心肌纤维化、心肌肥厚等病理过程中的作用,证明了micro RNA 可能作为心脏疾病治疗的候选RNA分子。近期研究发现长链非编码RNA对压力应激引起的心肌肥厚具有重要调控作用。包括LncRNA KCND1、Ak084656、Gm20257在小鼠心肌肥厚的病理过程中发挥重要作用,揭示了其作用机制和下游靶点,揭示了其作用机制和下游靶点,为药物作用机制研究开辟新的思路、新的药物作用靶点的发现。
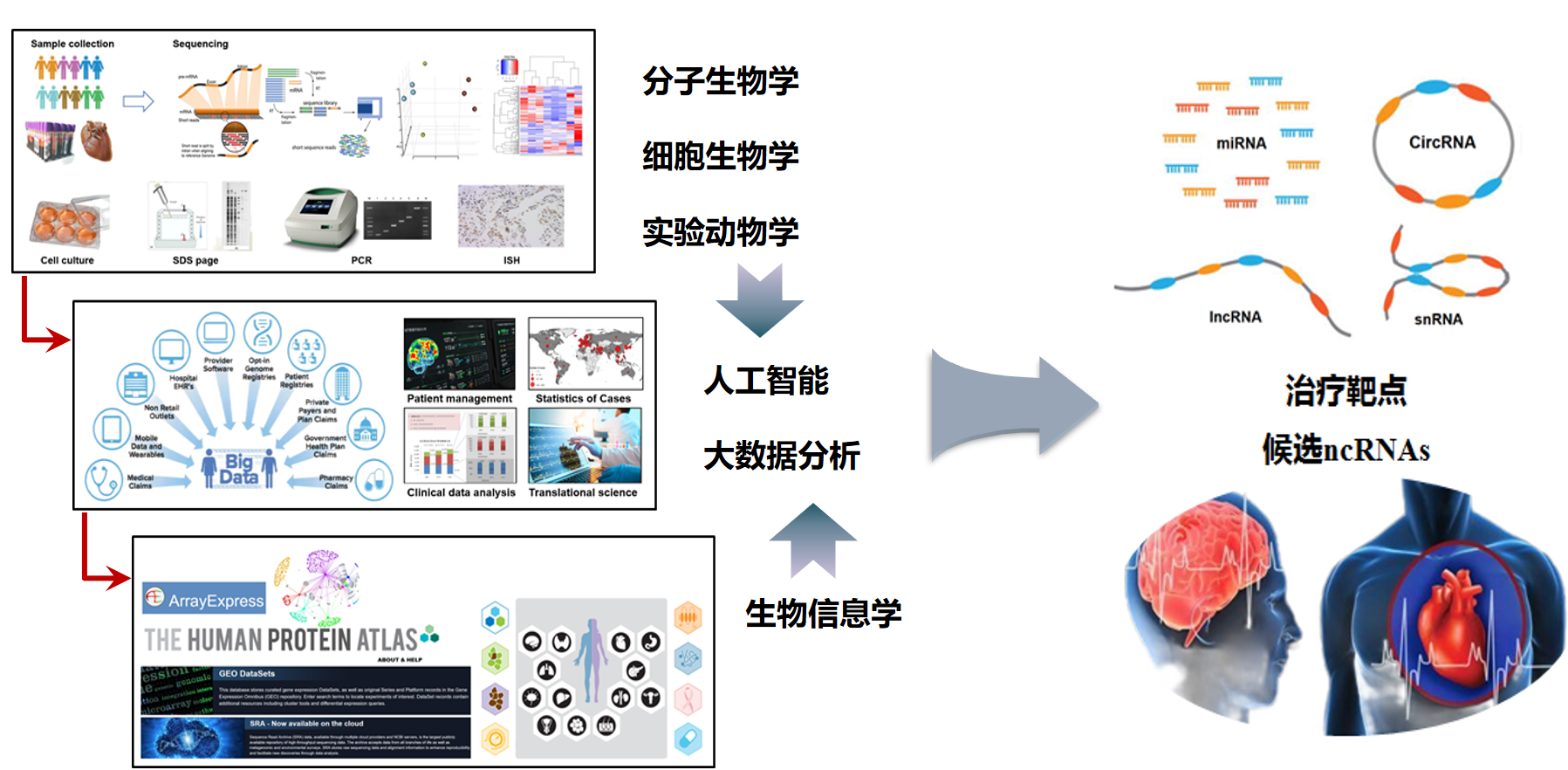
研究方向2:药物作用靶点的机制研究
探索心肌肥厚、心肌缺血再灌注损伤、心律失常等心脏重大疾病的药物作用靶点,发现NAP1l1、NET1、SerpinE2、ITFG2等潜在靶点,揭示以上靶点在心脏损伤调控过程中的分子机制;基于分子对接分子动力学模拟、热力学积分、自由能计算研究小分子与潜在作用靶点的相互作用,为药物开发提供新思路。
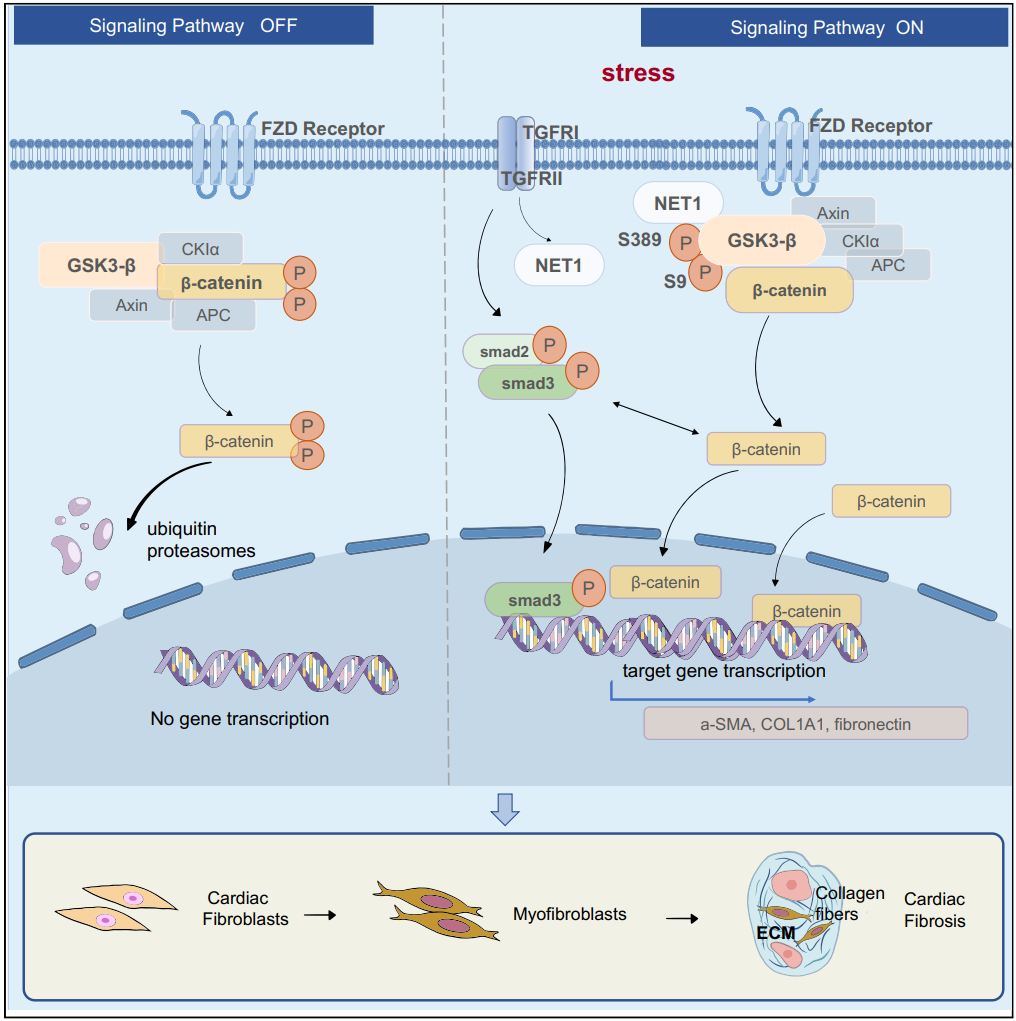
研究方向3:肿瘤药理学
探索在非小细胞肺癌、卵巢癌等恶性肿瘤进展中起关键作用的药物作用靶点,发现YAP1、长链非编码RNA PTAL等潜在靶点,并揭示其作用机制;利用生物医药虚拟筛选与智能平台,筛选潜在靶向肿瘤的药物分子,进行抗肿瘤药效评价及作用机制研究,为新型抗肿瘤药物研发提供新靶点。
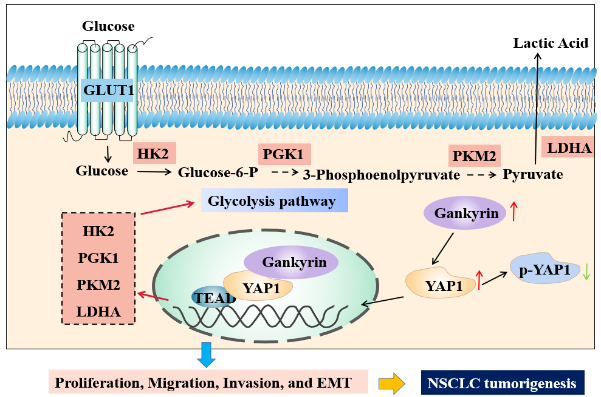
研究方向4:非编码RNA成药性研究
结合已经有的实验研究、整合公开数据库资源,利用人工智能预测筛选高效治疗心血管疾病、肺纤维化、肿瘤等重大疾病的非编码RNA,对非编码RNA药效、药理及毒理学进行评价;利用病灶部位特殊的微环境因子、受体与配体高亲和性以及递送材料与外部信号之间的主客效应,构建系列智能药物递送系统,为非编码RNA药物的开发提供理论支撑。
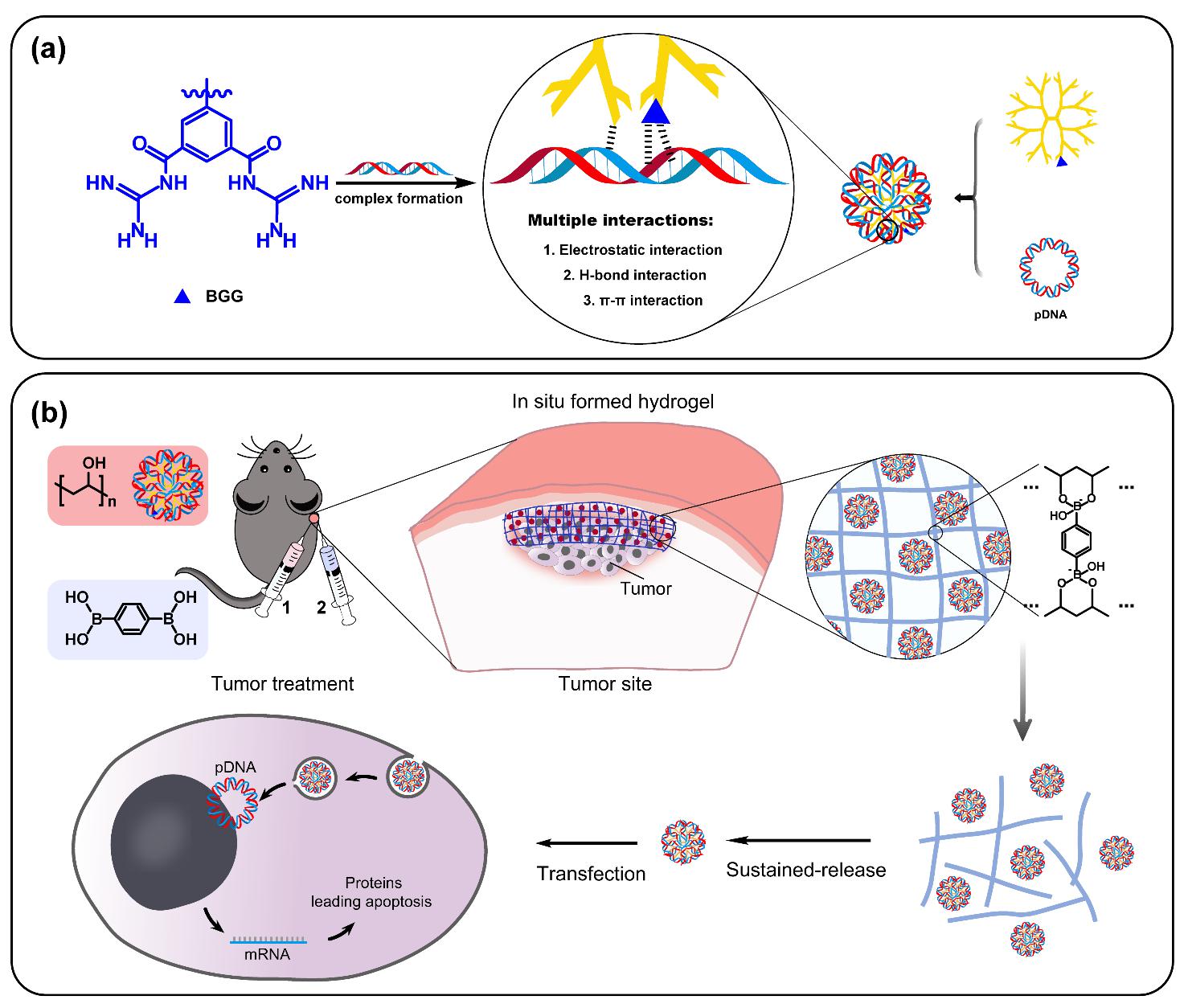
研究方向5:生物医学智能检测和医用机器人、医疗器械
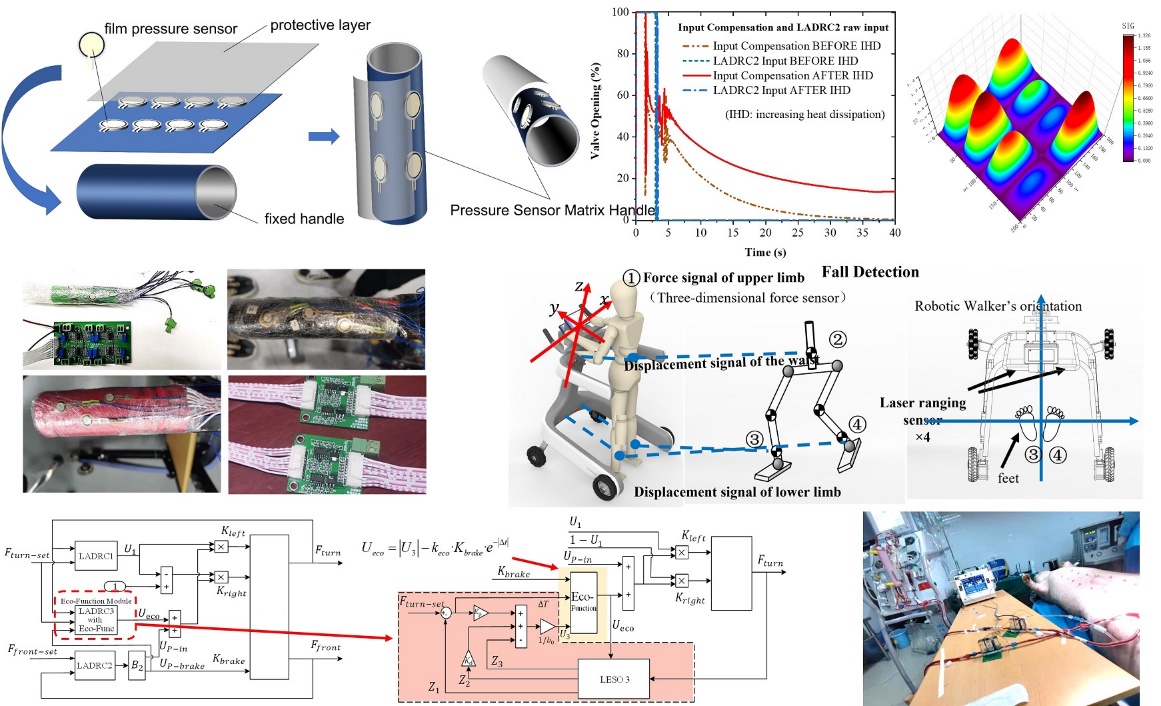
我国《“十四五”医疗装备产业发展规划》中明确指出:推进智能化、远程化、小型化、快速化、精准化、多模态融合、诊疗一体化发展,是我国当前医疗装备发展的一个重要方向;支持医疗装备、医疗机构、电子信息、互联网等跨领域、跨行业深度合作,鼓励医疗装备集成5G医疗行业模组,嵌入人工智能、工业互联网、云计算等新技术,推动医疗装备智能化、精准化、网络化发展,是目前前沿医疗装备、医疗仪器开发的有力的政策支撑。该研究方向聚焦于生物传感器研究、生物医学智能检测、可穿戴超声等医用装备和机器人开发、医疗图像处理、医用机器人智能控制等。
二、团队成员:
1 |
| 单宏丽:女,二级教授,博士, 中国协和医科大学 药理学专业 Email: shanhl@sues.edu.cn 主要从事心血管疾病发病机制、防治及药物靶点的研究,重点致力于探索微小核苷酸对心脏生理及病理过程的调控机制,并基于此寻找重大心血管疾病新的药物治疗靶点。尤其是近几年,系统阐释了非编码RNA(Non-coding RNAs,ncRNAs)在心肌电重构和结构重构中的作用机制,评价了ncRNAs作为心血管疾病治疗策略的可行性。主持完成973、国家自然科学基金等课题10余项,共发表研究论文110余篇,其中在Circulation、J Clin Invest、Cardiovascular Research等国际知名杂志发表SCI收录论文70余篇。获教育部科技进步一等奖及其他省部级奖项八项。 |
2 |
| 于桐:女,讲师,博士, 哈尔滨医科大学 药理学专业 Email: yutongyt@sues.edu.cn 主要从事非编码RNA在心脏损伤和肿瘤疾病中的机制研究,致力于寻找新的干预靶点和治疗药物,在MedComm、Cell Death and Discovery、British Journal of Cancer、FASEB J等杂志上累计发表科研论文15篇。参与国家自然科学基金重点项目1项,面上项目1项,上海市基地建设项目1项。 |
3 |
| 蒋淑侠:女,讲师,博士 南京农业大学,动物医学专业 主要从事非编码RNA和小分子化合物在肺纤维化和肿瘤疾病中的机制研究,在国际学术期刊累计发表科研论文8篇,其中第一作者发表SCI收录文章4篇。 |
4 |
| 丁大民:男,讲师,博士 上海理工大学 控制科学与工程专业 Email: dingdm@sues.edu.cn 主要研究方向纵向为生物传感器研究、可穿戴超声等医用装备和机器人开发、医疗图像处理、ADRC自抗扰控制等;横向主要从事医疗器械开发、光电智能仪器设计及制造、电气智能检测设备开发、数字信号分析与处理、模式识别系统开发等,在电路设计、单片机及DSP开发、PLC控制、LabVIEW编程等领域具有丰富的产品设计和设备开发经验。近年来先后在Nuclear Engineering and Technology等国际学术期刊上发表SCI论文4篇,国家专利授权1项。参与国家重点研发计划项目1项、国自然面上项目1项,上海市科委科技支撑项目和科技创新行动计划2项。 |
三、研究成果:
Neuroepithelial cell-transforming 1 promotes cardiac fibrosis via the Wnt/β-catenin signaling pathway. iScience, 26(10), 107888. doi:10.1016/j.isci.2023.107888
Nucleosome assembly protein 1 like 1 (NAP1L1) promotes cardiac fibrosis by inhibiting YAP1 ubiquitination and degradation. MedComm (2020), 2023 Aug 15;4(5):e348. doi: 10.1002/mco2.348. PMID: 37593048; PMCID: PMC10427634.
Substrate-dependent interaction of SPOP and RACK1 aggravates cardiac fibrosis following myocardial infarction. Cell Chem Biol. 2023 Jun 27:S2451-9456(23)00192-7. doi: 10.1016/j.chembiol.2023.06.015.
Long non-coding RNA KCND1 protects hearts from hypertrophy by targeting YBX1. Cell Death Dis. 2023 May 30;14(5):344. doi: 10.1038/s41419-023-05852-7.
Interdependent Nuclear Co-Trafficking of ASPP1 and p53 Aggravates Cardiac Ischemia/Reperfusion Injury. Circ Res. 2023 Jan 20;132(2):208-222. doi: 10.1161/CIRCRESAHA.122.321153.
Endocytosis of Peptidase Inhibitor SerpinE2 promotes Myocardial Fibrosis through activating ERK1/2 and β-catenin Signaling Pathways.International Journal of Biological Sciences.2022; 18(15): 6008-6019. doi: 10.7150/ijbs.67726.
Critical role of PAFR/YAP1 positive feedback loop in cardiac fibrosis. Acta Pharmacol Sin. 2022 Nov;43(11):2862-2872. doi: 10.1038/s41401-022-00903-9.PMID: 35396533.
LncRNA DACH1 protects against pulmonary fibrosis by binding to SRSF1 to suppress CTNNB1 accumulation. Acta Pharm Sin B. 2022 Sep;12(9):3602-3617. doi: 10.1016/j.apsb.2022.04.006.
Montelukast, cysteinyl leukotriene receptor 1 antagonist, inhibits cardiac fibrosis by activating APJ. Eur J Pharmacol. 2022 May 15;923:174892. doi: 10.1016/j.ejphar.2022.174892.
The Facile Preparation of PBA-GO-CuO-Modified Electrochemical Biosensor Used for the Measurement of α-Amylase Inhibitors' Activity. Molecules. 2022 Apr 7;27(8):2395. doi: 10.3390/molecules27082395.
Construction of ultrasound-responsive urokinase precise controlled-release nanoliposome applied for thrombolysis. Front Bioeng Biotechnol. 2022 Aug 9;10:923365. doi: 10.3389/fbioe.2022.923365.
Gankyrin modulated non-small cell lung cancer progression via glycolysis metabolism in a YAP1-dependent manner. Cell Death Discov, 8(1), 312. doi:10.1038/s41420-022-01104-3
Cytoplasmic sequestration of p53 by lncRNA-CIRPIL alleviates myocardial ischemia/reperfusion injury. Commun Biol, 5(1), 716. doi:10.1038/s42003-022-03651-y
科研项目
1.上海市心脑血管非编码RNA成药性前沿科学研究基地(培育)。
2.国家自然科学基金面上项目,NAP1L1调控Hippo/YAP1通路参与心肌纤维化的机制研究。
3.黑龙江省自然科学基金重点,心肌梗死的新机制:A lncRNA 对溶酶体- - 线粒体网络的调控作用。
4.国家自然科学基金面上项目,线粒体自噬新的调控分子:lncRNAs及其生物网络构建。
5.国家自然科学基金应急管理项,长链非编码RNA参与心肌自噬的发生及其机制研究。
6.黑龙江省杰出青年科学基金项,微小核苷酸分子在重大心脏疾病中调控机制。
7.国家重点基础研究发展计划(973项目),心肌细胞内物流系统的表观遗传学调控。
四、仪器设备:
多功能成像仪 | 小动物活体成像系统 | 实时荧光定量PCR仪 |
双色红外激光成像系统 | 流式细胞仪 | 荧光显微镜 |
组织破碎仪 | 扫描电子显微镜 | 百万分之一天平 |
全功能酶标仪 | 超纯水系统 |




